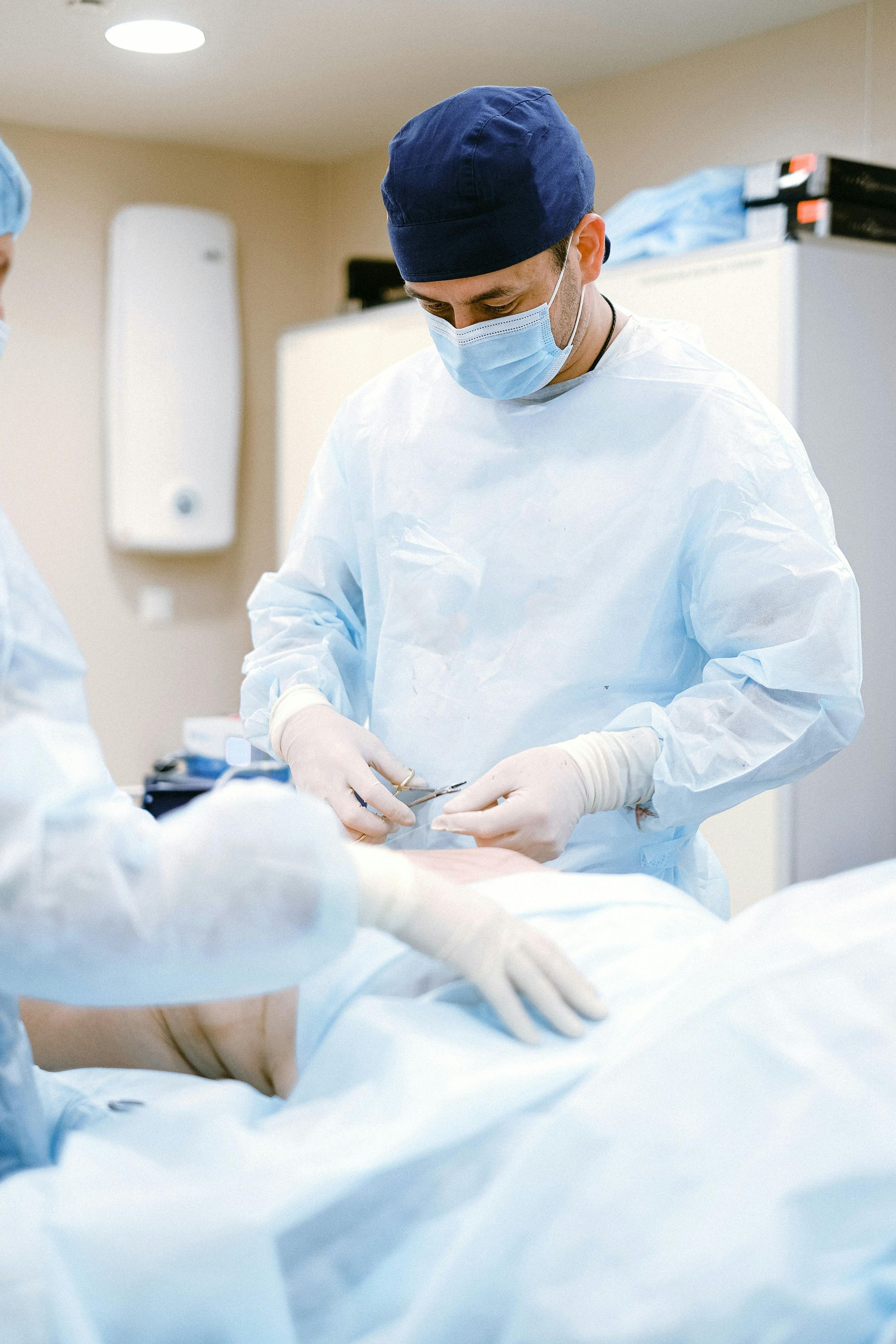
Testosteron og Type 2-diabetes: Den oversete sammenhæng med klinisk potentiale
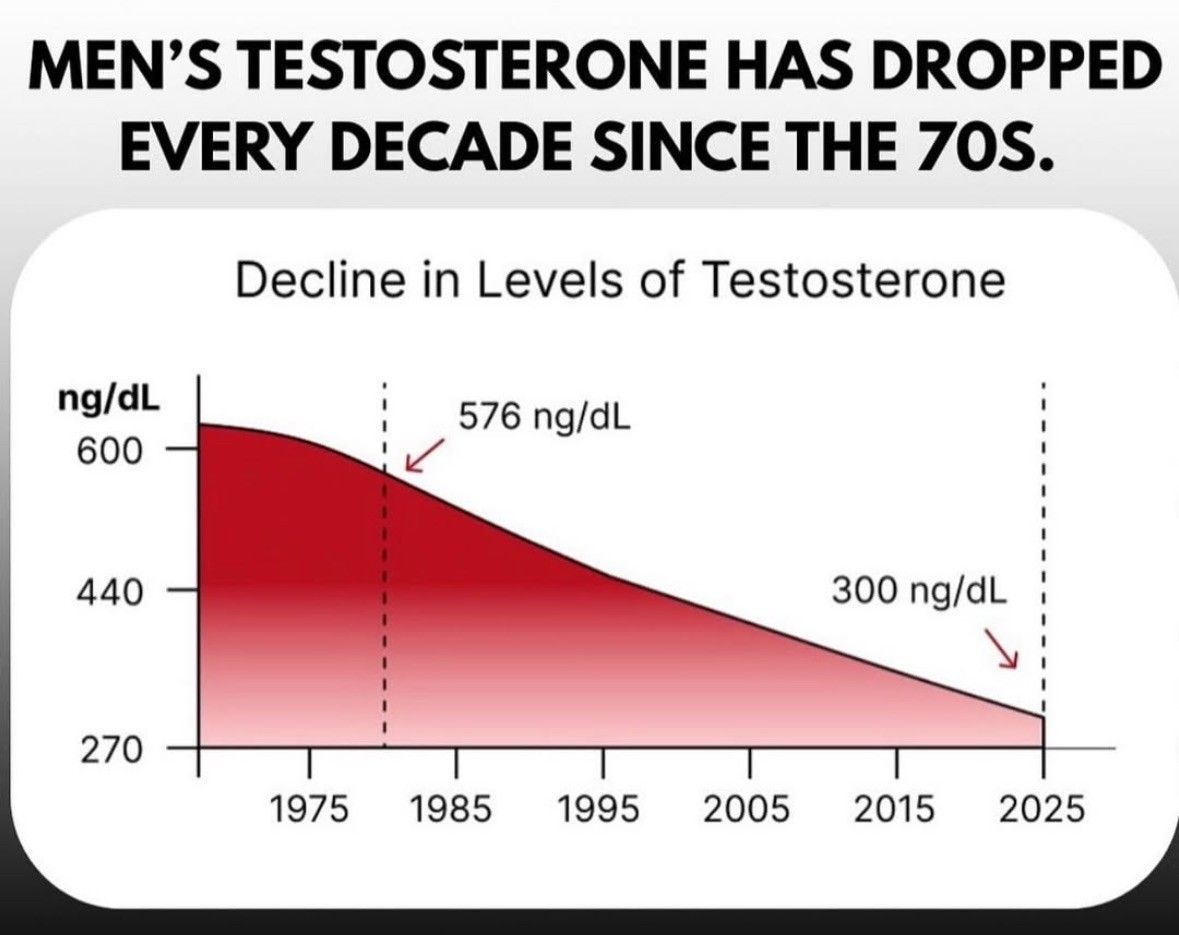
Den globale stigning i type 2-diabetes (T2D) ledsages af faldende testosteronniveauer hos mænd. Forskningen påviser nu tydeligt, at disse fænomener ikke blot forekommer samtidigt – de er dybt forbundne. Lavt testosteron fungerer ikke kun som en konsekvens af metabolisk sygdom, men spiller også en aktiv rolle i udviklingen og forværringen af insulinresistens.
I dette indlæg afdækkes den bi-direktionelle sammenhæng mellem testosteron og T2D, patofysiologien bag, det kliniske potentiale ved målrettet testosteronterapi samt betydningen af livsstilsfaktorer og integrativ behandling.
1. En bi‑direktionel sammenhæng
Adskillige studier har påvist, at lavt testosteron hos mænd er forbundet med øget risiko for insulinresistens og udvikling af type 2-diabetes, uanset alder og BMI. Op mod 30–50 % af mænd med T2D lider af uerkendt hypogonadisme – ofte uden klare symptomer. Et klinisk eksempel illustrerer, hvordan en 54-årig mand med prædiabetes, abdominal fedme og lavt testosteronniveau oplever forbedret insulinfølsomhed og reduktion i HbA1c efter seks måneders kostintervention, motion, tilskud og testosteronterapi.
2. Patofysiologi: Mekanismer bag testosteronfald og metabolisk betydning
Testosteron er centralt for glukosemetabolisme, fedtforbrænding og mitokondriefunktion. Det øger insulinfølsomhed via GLUT4-aktivitet, fremmer muskelmasse og reducerer visceralt fedt og inflammation. Ved mangel på testosteron ses en effektiv kaskade af negative effekter: øget fedtlagring, leptinresistens, nedsat adiponectin og højere proinflammatoriske cytokiner som TNF-α og IL-6 – faktorer direkte koblet til insulinresistens og mitokondriel svækkelse.
3. Livsstilsdeterminanter: Årsager til testosteronfald og metabolisk dysfunktion
Ud over naturlig aldring bidrager flere moderne livsstilsfaktorer til fald i testosteron og stigende T2D-prævalens. Kost rig på ultraforarbejdede fødevarer, raffinerede kulhydrater og omega‑6-olier fremmer inflammation og hormonforstyrrelse, mens fysisk inaktivitet reducerer muskelmasse og insulinfølsomhed. Kronisk inflammation svækker spermie‑ og testosteronproduktion, ligesom hormonforstyrrende kemikalier som ftalater, bisfenol A og pesticider påvirker syntesen negativt. Mangel på vigtige mikronæringsstoffer såsom zink, magnesium, D-vitamin og B6 forstærker desuden både testosteronmangel og metabolisk dysfunktion. Endelig bidrager alkohol og rekreative stoffer med dokumenteret effekt på hormonhæmning, insulinresistens og leverfunktion, inklusiv cannabis, opioider og benzodiazepiner.
4. Evidens overbeviser: Testosteron og diabetesstudier
Nyere studier understøtter den kliniske relevans. European Male Aging Study fandt, at lavt frit testosteron forudsiger T2D, uafhængigt af BMI og alder. T4DM-studiet viste, at testosteronterapi reducerede risikoen for T2D med 41 % over to år hos mænd med prædiabetes og lavt testosteron, uden alvorlige bivirkninger. Desuden viste NHANES III-data, at mænd med total testosteron <10 nmol/L havde 2–3 gange øget T2D-prævalens, trods justering for øvrige faktorer.
5. Klinisk implikation: Skal vi screene bredere?
Det korte svar er ja. Mænd med T2D, prædiabetes eller metabolisk syndrom bør rutinemæssigt screenes for testosteronmangel – især ved symptomer som kronisk træthed, nedsat libido, central fedme og erektil dysfunktion. Et anbefalet testpanel bør omfatte total testosteron, SHBG, albumin, LH, FSH, prolaktin, HbA1c, insulin, HOMA-IR samt vigtige mikronæringsstoffer.
6. Terapeutisk potentiale: Testosteronterapi som metabolisk intervention
Hos mænd med biokemisk og klinisk hypogonadisme – uden kontraindikationer – kan testosteronterapi forbedre insulinfølsomhed, reducere visceralt fedt og fedtlever, fremme muskelmasse og fysisk kapacitet samt øge kognition, libido og livskvalitet. Behandlingen kræver tæt opfølgning, eksempelvis hæmatokrit, PSA, lipidstatus og leverparametre, samt fortsat fokus på livsstilsoptimering og mikronæringsstoffer.
7. Konklusion
Det er ikke kun alderen, men metabolisk dysfunktion, der driver testosteronnedgangen hos mænd. Kombinationen af lavt testosteron og T2D skaber en inflammatorisk og hormonel spiral, som kræver tidlig indsats. Ved at integrere livsstilsændringer, mikronæringsstofkorrektion og – når indiceret – testosteronterapi, opnås en helhedsorienteret, evidensbaseret tilgang til behandling og forebyggelse af insulinresistens og hypogonadisme.
Referencer (udvalgte)
Grossmann M. Testosterone and glucose metabolism in men. Diabetes & Metabolism, 2014
T4DM Study Group. Testosterone treatment and type 2 diabetes prevention in men with low testosterone and prediabetes (T4DM). Lancet Diabetes Endocrinol. 2021;9(2):98–110
Antonio L et al. The European Male Aging Study. J Clin Endocrinol Metab. 2015;100(4):1394–1401
Ruiz‑Núñez B et al. Lifestyle and low‑grade inflammation in the pathogenesis of chronic disease. Am J Clin Nutr. 2016;104(Suppl 1):128–33
Kelly DM, Jones TH. Testosterone and inflammation in men with low testosterone levels. Endocr Rev. 2013;34(5):598–618
Pilz S et al. Vitamin D and testosterone in men. Nat Rev Endocrinol. 2011;7(12):667–76
Meeker JD et al. Environmental exposures and male reproductive health. Environ Health Perspect. 2010;118(9):1265–72
Andersen ML et al. Testosterone and alcohol: from basic research to clinical perspectives. Alcohol Research. 2016;38(2):289–306
Hall W et al. Cannabis use and male reproductive hormones: systematic review and meta‑analysis. J Clin Endocrinol Metab. 2008;93(11):4202–09